CAR-T细胞疗法的内在耐药机制
嵌合抗原受体(CAR)T细胞疗法已成为癌症治疗的新机遇,然而,由于内在的CAR结构及T细胞、外在肿瘤或微环境因素,可能会出现耐药性。在许多情况下,对这些机制的了解来自于接受CAR-T细胞治疗患者的临床观察。CAR的分子结构和制造工艺也会影响CAR-T细胞的疗效,肿瘤细胞或肿瘤微环境中的突变等外在因素也会影响。肿瘤细胞会出现获得性抗原丢失或异质性,从而能够抵抗CAR-T细胞杀伤。此外,骨髓细胞、调节性T细胞和成纤维细胞可以发挥免疫抑制作用并消除CAR-T细胞的抗肿瘤功效。这里我们将讨论内在耐药机制以及克服的新方法,促使CAR-T癌症疗法能够广泛应用。
接受CAR-T细胞治疗的患者需分离获得T细胞,然后利用CAR转基因扩增制造输注的产品。这个过程中会出现许多问题,如所需的最低T细胞数量、T细胞状态以及CAR-T细胞产品的保存,这些都与体外扩增、转导效率、细胞毒性能力、分化状况和患者反应率有关,CAR的转基因方法设计也会影响其疗效和持久性。图1描述了CAR-T细胞的制造和优化过程。
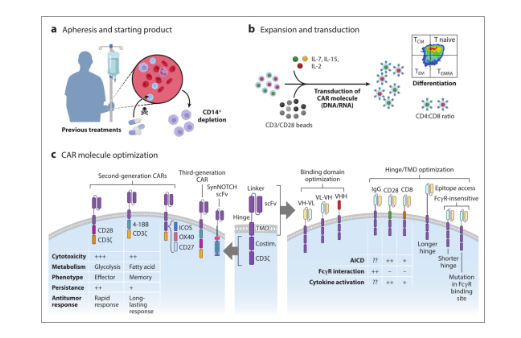
CAR-T细胞疗法的内在耐药性以及提高其疗效的方法。(a) 单采过程和起始状态会影响产品的最终质量,先前的化疗会影响免疫细胞功能。(b)使用不同细胞因子的扩增会改变最终产品中CAR-T细胞的表型。具有干细胞中央记忆表型和相等CD4:CD8比率的CAR-T细胞产品与更好的结果相关。(c) CAR结构优化可以针对特定肿瘤类型实现理想的疗效。
起始细胞和离体激活扩增
CAR-T细胞制造首先从患者体内单采PBMC,一般以每微升T细胞数量来表示,有研究人员可以从至少150个 CD3 +细胞/μL开始生产CAR-T细胞,目前还没有研究确定能够成功生产的最低细胞数量。在此过程中,使用细胞因子和刺激磁珠的不同组合来优化最终产品中 CAR-T细胞的数量和表型。最常用的细胞因子是IL-2、IL-7和IL-15与抗CD3/CD28抗体磁珠的组合。IL-7和IL-15可以刺激呈现出更多的干记忆表型,并且扩增CAR-T细胞往往具有更高的细胞毒性。另外还有IL-4 和TGF-β等细胞因子的组合,当这些细胞因子结合在一起时,会在CAR-T细胞中诱导Th9表型,分泌 IL-9。IL-9对免疫系统具有多效性作用,可以作为一种免疫抑制细胞因子,刺激肥大细胞和Treg 并限制抗原呈递细胞的功能诱导Th1反应,另外还可以作为自身免疫和过敏性疾病中的促炎细胞因子。分泌IL-9的CAR-T细胞与用IL-2和CD3/CD28磁珠扩增的传统Th1 CAR-T 细胞相比,在体外和体内具有更高的抗肿瘤活性,从而导致较少的T细胞耗竭和分化。
T细胞表型
CAR-T细胞表型与CAR-T细胞治疗的临床疗效相关。在单采血液中存在的不同 T 细胞表型中,具有记忆样特征的T细胞表型具有更好的体外和临床效果,其中CD8+ CAR-T细胞的记忆特征(CCR7、CD27和SELL表达较高)与完全缓解(CR) 相关,记忆样T细胞 (CD27+、CD45RO−、CD8+)的数量也与持续缓解呈正相关。在T细胞记忆亚型中,中枢记忆表型比效应记忆表型具有更高的体内和体外活性。
当源自幼稚T细胞时,使用IL-7、IL-21和糖原合酶3b抑制剂的组合刺激,可以产生具有中央记忆 (TSCM )表型的CAR-T 细胞,这些细胞更具活力和更持久的杀伤活性,有利于分离T细胞较少的患者。此外,用IL-7和IL-15进行体外培养可部分恢复TSCM的数量。有研究表明TSCM细胞似乎在早期抗白血病反应阶段至关重要,因为它们能够转变为中枢记忆T细胞和效应记忆T细胞。由于它们的自我更新能力,也与CAR-T细胞的长期持续存在相关。
CD4与CD8 细胞比例
CAR-T细胞制造过程中需要考虑的另一个因素是CD8与CD4 CAR-T 细胞的最佳比例。两种可以同时扩增,但最终产品中比例的差异可能会影响临床结果。体内实验表明,开始CAR-T细胞扩增的最佳比例是CD4+与CD8+ T细胞的比例为 1:1。使用1:1比例的CD4:CD8 CD19靶向CAR-T细胞作为起始产品是可行的,并且可以将获得临床反应所需的输注细胞量减少5至100倍。该产品是百时美施贵宝开发的Breyanzi(liso-cel),2021年经 FDA批准用于治疗复发或难治性大B细胞淋巴瘤患者。

在最近一项针对ALL的抗CD22 CAR临床试验中,在单采后进行CD8/CD4细胞富集过程提高了转导效率、离体扩增和患者体内的持久性,从而减少了所需CAR-T细胞的数量以获得临床反应。这些数据表明,在制造过程中选择均衡且富含TSCM的T细胞群可以在抗肿瘤功效方面带来更好的临床结果。
单核细胞的作用
单采旨在收集单核细胞,包括淋巴细胞和单核细胞。单核细胞可以吞噬CD3/CD28激活磁珠,从而损害T细胞激活和转导。当PBMC中CD14+单核细胞被耗尽时,在扩增、转导效率、细胞毒性和中央记忆表型方面效果会增加。监测单采产品中CD14 +细胞的数量可以避免其对CAR-T细胞生产的有害影响。有学者提出单采血液成分中单核细胞含量的最大阈值为40%,作为CAR-T细胞生产的质量控制,使用特异性吸附和逆流离心可以去除单核细胞。
化疗对CAR-T细胞的影响
大多数接受CAR-T细胞治疗的患者都或多火杀接受过多种化疗,这些化疗可能会影响他们的PBMC数量和T细胞表型。CTX和AraC化疗会导致TSCM和幼稚T细胞减少。潜在的恶性肿瘤也会影响T细胞的绝对数量,从而影响T细胞的扩增。例如,患有慢性淋巴细胞白血病(CLL)或 ALL的患者通常表现出白细胞增多,但这通常是循环恶性B细胞疾病的结果,并且存活的功能性T细胞数量较低。淋巴瘤患者通常也存在功能性T细胞缺陷,而MM或大多数实体瘤类型(胶质母细胞瘤、卵巢癌、前列腺癌和间皮瘤)患者即使在轻度或中度淋巴细胞减少的情况下还具有功能性T细胞。
淋巴细胞清除或预处理方案通常在T细胞采集后和CAR-T输注前进行,减少Treg细胞和骨髓抑制细胞,为输注CAR-T细胞腾出空间。此外,一些细胞因子(如IL-15)在淋巴细胞清除后增加,促进输注细胞的扩增。使用氟达拉滨(FA)和CTX进行淋巴细胞清除可增加CAR-T细胞的扩增、持久性和临床反应,这可能是由于最大限度地减少了针对CD19特异性CAR 中单链可变片段 (scFv) 的鼠源部分的免疫T细胞。在胰腺癌和前列腺癌的小鼠模型中,使用CTX预处理可改变TME为更具促炎性的状态,同时增加抗原呈递细胞和T细胞的募集,改善长期肿瘤控制。
优化CAR的结构设计
CAR分子包含三个主要部分:抗原结合域、铰链区和跨膜结构域以及胞内结构域,每一部分的设计都关系到CAR的功能和功效。尽管抗原结合域或胞内结构域似乎在 CAR 疗法中具有更大的相关性,但铰链区和scFv之间连接子的长度和组成也可以增强或减弱CAR活性。
抗原结合域
抗原结合域包含特异性靶向肿瘤抗原的scFv,开发更有效的scFv序列的新策略包括将已知的肿瘤抗体可变区与人重链和轻链的可变区和J区文库组合来生成scFv文库,从而筛选出更特异的CAR 分子,增加CAR-T细胞的增殖、耐久性和体内抗肿瘤活性。另外,scFv的亲和力与靶向肿瘤外毒性有关。使用较低亲和力可以将CAR-T细胞重定向到靶向抗原更密集的区域(即肿瘤细胞),特别是该抗原在健康细胞上表达水平较低时。
尽管VL和VH链之间的连接肽通常是惰性的,但它仍然可以影响抗原识别。较短的连接子导致分子间配对(相对于分子内配对),这意味着对目标抗原的亲和力稍高。由于这些分子间相互作用,较短的接头可以更容易地建立CAR簇,从而增加来自受




